Es wird ja immer wieder behauptet, es gäbe keine Forschungsergebnisse zur Homöopathie. Diese Behauptung ist falsch. Das zeigen auch eine Reihe klassischer klinischer Studien. Klassisch deshalb, weil sie schon vor geraumer Zeit durchgeführt wurden und oft zitiert werden.
Homöopathie bei Heuschnupfen –
zwei randomisierte, placebokontrollierte Doppelblindstudien
Harald Walach
Reilly, D. T., & Taylor, M. A. (1985). Potent placebo or potency? A porposed study model with initial findings using homeopathically prepared pollens in hayfever. The British Homoeopathic Journal, 74, 65-75.
Reilly, D. T., Taylor, M. A., Mc Sharry, C., & Aitchinson, T. (1986). Is homoeopathy a placebo response? Controlled trial of homoeopathic potency with pollen in hayfever as a model. Lancet, Oct. 18, 881-886.
Die Heuschnupfenperiode hat begonnen. Pollen fliegen, Nasen tropfen, Augen weinen. Dagegen gibt es wenig Hilfe. Man kann die Symptome bekämpfen und Antihistaminika nehmen. Sie reduzieren die allergische Reaktion des Körpers auf die Antigene der Pollen, ändern aber nichts an der Empfindlichkeit, und bei vielen Menschen lösen sie unangenehme Nebenwirkungen wie Müdigkeit aus. Man kann den Weg der immunologischen Desensibilisierung beschreiten. Dabei werden die entsprechenden Antigene zunächst ausfindig gemacht und dann dem Körper in einer Art umgekehrter Homöopathie von der gerade noch harmlosen über eine aufsteigende Dosisreihe präsentiert, in der Hoffnung, dass damit die Sensitivität verschwindet und der Körper sich anpasst. Das hilft auch vielen. Aber nicht allen. Wenn diese Methode nichts hilft, dann bleibt die Homöopathie.
An dieser Stelle kommen David Reillys Studien ins Spiel. Ich habe den Autor 1985 einmal auf einer Tagung in London erlebt, wie er seine Studien vorgestellt hat. Die Idee sei ihm gekommen, als er in einer Apotheke Nelson’s „Mixed Grasspollen C30“ gesehen habe, ein homöopathisches Fertigpräparat zur Behandlung allergischer Rhinitis, also Pollenallergie. Darin enthalten sind die 24 häufigsten Pollenallergene von Gräsern, potenziert zur C30, also eine „Verdünnung“ von 100-30 oder 10-60. Unter molekularen Gesichtspunkten ist das eine absurd niedrige Verdünnung, bei der statistisch kein Molekül mehr vorhanden ist, weil die Avogadrosche Zahl (ungefähr 10-23) längst unterschritten ist; die gibt an, bei welcher Verdünnung noch mit einem Molekül zu rechnen ist. Wenn eine solche Potenz eine Wirkung entfaltet, dann sicher nicht über die vorhandenen Moleküle sondern über andere Prozesse. Zumal man ja bedenken muss, dass bei dem Herstellungsprozess die Ursprungslösung noch auf Zuckerkügelchen, oder in diesem Falle auf Milchzuckertabletten aufgeträufelt wird in einem Sprühverfahren, bei dem zwar alle Tabletten oder Kügelchen erreicht werden – das wurde bereits öfter untersucht. Aber die Menge der Ausgangslösung ist extrem gering. Die Wahrscheinlichkeit, dass also irgendein Molekül der Ausgangslösung beim Patienten ankommt ist praktisch gleich Null. Daher ja der Disput. Kann nicht wirken, sagen klassische Pharmakologen, Kritiker und Wissenschaftler. Wirkt eben doch, zeigt die Praxis – und eben auch die Forschung.
David Reilly hat zwei verblindete, placebo-kontrollierte, randomisierte klimische Studien mit einem sehr ähnlichen Aufbau durchgeführt. Die erste war eine Pilotstudie und diente der Klärung der Frage, ob sich dieses Modell überhaupt lohnt. Dabei wurde eine kleine Zahl von Patienten, insgesamt 13 in der Homöopathie und 26 in der Placebo-Gruppe, behandelt. Die ungleichen Zahlen kamen daher, dass die Vorbereitung der Präparate in Paaren geschah, das erste Glas immer Placebo enthielt, ohne dass das jemand wusste (außer dem Apotheker), und das zweite Verum. Die Idee war, dass dadurch nach Möglichkeit immer zeitnahe Paare eingeschlossen werden sollten, um zeitliche und lokale Schwankungen im Pollenflug experimentell auszugleichen. Da manche Ärzte aber mehrere Patienten einschlossen (und damit immer wieder ein neues Paar anfing), ergaben sich oft ungerade Zahlen und daraus diese Imbalance.
Die Patienten durften keine Erfahrung mit Homöopathie haben, mussten eine dokumentierte 2jährige Geschichte mit Pollenallergie haben, akute Symptome, keine Infekte, und keine relevante Vormedikation mit konventioneller Therapie mit entsprechenden Karenzfristen für Medikamente. Diese Kriterien wurden in der Hauptstudie noch verschärft dahingehend, dass auch ein immunologischer IgE-Antikörpertest gegen Pollen vorliegen musste. Die eingeschlossenen Patienten waren also wirklich Pollenallergiker.
Gemessen wurde in beiden Studien über Patiententagebücher:
Zum einen wurde eine visuelle Analogskala erfasst, die die Gesamtbelastung durch die Symptome abbilden sollte. Das ist ein 10cm langer Stricht, vergleichbar einem Thermometer. Auf ihm gibt der Patient durch Ankreuzen täglich an, wie belastend die Symptome sind zwischen „überhaupt nicht“ und „extrem“. Man misst dann die Länge des Strichs und diese dient als Masszahl. Solche Skalen sind in der Forschung seit langer Zeit üblich und sehr sensibel. Außerdem wurden die 6 wichtigsten Symptome im Tagebuch erfasst (Niesen, laufende und juckende Nase, rote, tränende und schmerzende Augen), die in der Pilotstudie mit einem dreistufigen und in der Hauptstudie mit einem vierstufigen Rating einzustufen waren. Zusätzlich wurde die Menge an Ausweichmedikation erfasst. Dazu war ein Antihistaminikum für alle vorgesehen.
Die Medikamente wurden 2mal täglich über 2 Wochen eingenommen und noch 2 Wochen nachbeobachtet. In der Hauptstudie wurde zusätzlich eine einwöchige Placebo-Run-in-Phase eingeführt, um eine Baseline zu haben, also einen Ausgangswert, gegen den Veränderungen berechenbar sind.
Schon die Pilotstudie hatte deutliche Effekte gezeigt, die mit einem robusten, non-parametrischen statistischen Test signifikant waren. Die Homöopathie-Gruppe verbesserte sich um 80%, die Placebo-Gruppe um 18%. Dabei hatten die Homöopathie-Patienten tendenziell weniger Antihistaminika eingenommen als die Placebo-Patienten. Auch waren aus der Homöopathie-Gruppe weniger Patienten wegen irgendwelcher Verschlimmerungen oder Unverträglichkeiten ausgeschieden als aus der Placebogruppe. Die Pilotstudie war also vielversprechend.
In der Hauptstudie konnten nun die Ergebnisse sehr deutlich repliziert werden. Die Stichprobe war deutlich grösser: 158 Patienten, 79 in jeder Gruppe, wurden behandelt. Die Behandlung fand in zwei Zentren, in Glasgow und in London, statt. Ausserdem wurden noch die Pollenflugdichten berechnet und in die Studie einbezogen. Durch die einwöchige Run-in-Phase, in der alle Patienten Placebo einnahmen, war auch eine Ausgangslage dokumentiert. Man hätte sich hier vielleicht eine Baseline ohne irgendeine Intervention gewünscht. Gegenüber dieser Baseline, die ja eigentlich schon psychologisch gesehen einen gewissen Behandlungseffekt gezeigt haben dürfte, wurden nun die Effekte berechnet.
Das Hauptzielkriterium in der Hauptstudie war die visuelle Analogskala der Symptombelastung. In der Homöopathiegruppe hatte diese nach 4 Wochen um 17,2 mm abgenommen, in der Placebogruppe um 2,6 mm. Das ist mit d = 0.47 eine mittelgroße, aber durchaus klinisch relevante Effektgrösse. Die Studie war statistisch mit einer Mächtigkeit versehen, die einen 10%igen Unterschied sichtbar machen sollte. Der Effekt hier ist leicht kleiner gewesen, aber er war statistisch signifikant. Eine Sensitivitätsanalyse führte dann noch eine Korrektur für die Pollenzählung durch und bestätigte den Effekt (Abbildung).
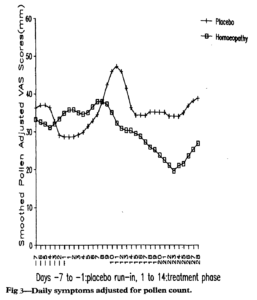
Die Patienten in der Homöopathie-Gruppe nahmen signifikant weniger Antihistaminika, nämlich 11,2 im Durchschnitt gegenüber 19,7 in der Placebogruppe. Das ist mit d = 0.5 eine mittelgrosse und klinisch relevante Effektgröße. Die Verbesserung in der Homöopathie-Gruppe ist also keinesfalls auf eine vermehrte Einnahme konventioneller Medikamente zurückzuführen.
Ein Manko ist aus meiner Sicht, dass die differenzierten Tagebuchdaten der 6 Symptome lt. Angaben im Methodenteil in einer anderen Publikation erscheinen sollten. Das ist aber meines Wissens nie geschehen. Möglicherweise waren die Daten dieser Tagebücher nicht ganz so eindeutig wie die VAS? Das könnte leicht sein. Darüber weiss ich aber nichts. Es ist für die Bewertung dieser Studie allerdings nicht sehr relevant, weil die VAS-Skala als Hauptzielkriterium formuliert worden war und einen deutlichen Effekt zeigt, der durch die Abnahme des Antihistaminika-Verbrauchs in der Homöopathiegruppe gegenüber der konventionellen Gruppe auch noch gestützt wird.
Insgesamt ist dies eine Serie von zwei Studien, die einen deutlichen und replizierten Effekt von homöopathisch hochverdünnten gemischten Graspollen in der C30 zeigt. Auch eine Verbesserung der Methodik in der zweiten Studie, wie etwa die Objektivierung der Allergie durch IgE und Rast-Testung oder der Einbezug der Pollenzählung hat dem Effekt keinen Abbruch getan. Die Effektgrössen sind in der Hauptstudie kleiner als in der Pilotstudie. Aber sie sind immer noch in einem Bereich, der sie klinisch relevant macht.
David Reilly hat in einer Studie mit einem anderen Modell – nämlich potenziertem individuellem Antigen bei Asthma – diese Serie fortgesetzt und damit den Effekt in einer konzeptuellen Replikation bestätigt [1]. Eine vierte Studie, dieses Mal wieder bei Heuschnupfen, konnte dann allerdings den Effekt nur noch indirekt bestätigen. [2] Denn hier war das primäre Zielkriterium, die visuelle Analogskala, nicht mehr signifikant. Dafür aber das sekundäre, nämlich der objektive Histaminverbrauch. Diese Studie hatte auch eine Meta-Analyse des Gesamteffektes durchgeführt und alle vier Studien zusammengefasst. Diese Meta-Analyse ist signifikant und zeigt einen gemittelten Effekt von 11.1 mm Verbesserung auf der visuellen Analogskala, also in etwa den Effekt, der auch in der hier besprochenen Hauptstudie dokumentiert wurde.
Diese beiden anderen Studien besprechen wir separat, weil sich an ihnen noch ein paar andere Dinge zeigen lassen. Wir sehen: homöopathische Therapie kann durchaus Effekte haben, die signifikant von Placebo verschieden sind. Auch wiederholt. Allerdings zeigen manchmal weitere Wiederholungen Kapriolen: Die Effekte springen plötzlich hinüber ins Nebenzielkriterium. Diese Situation erlaubt es jedem, sein eigenes Weltbild zu zimmern: Die Homöopathie ist nicht replizierbar, sagen dann die Kritiker. Sie haben, wie wir gesehen haben, nur teilweise recht. Manchmal ist sie in der Tat replizierbar. Manchmal nicht. Das ist allerdings das Schicksal guter Forschung. Nur wenige Befunde, auch in der konventionellen Forschung, sind wirklich strikt replizierbar. In der Homöpathieforschung ist Replizierbarkeit noch seltener. Diese Serie von zwei Studien zeigt, dass auch in der Homöopathie replizierbare Befunde vorliegen. Und in der Praxis erlaubt es dem rational gesinnten Allergiker durchaus, Homöopathie auszuprobieren. Möglicherweise hat er oder sie ja mit einer klassisch-homöopathischen Therapie sogar noch mehr Chancen? Denn vergessen wir nicht, dass hier ja ein relativ grober homöopathischer Ansatz getestet wurde.
An diesem Beispiel zeigt sich auch eine subtile Dialektik der Homöopathieforschung: Forschungslogisch sind diese beiden Studien sehr schön, weil klar, eindeutig, aufeinander aufbauend und repliziert. Praktisch sind sie relativ wenig interessant. Denn kaum ein Homöopath wird Heuschnupfen mit gemischten Gräserpollen behandeln, zumindest nicht in Deutschland und vermutlich auch anderswo nicht. Das hier verwendete Modell der Isopathie – also „Gleiches mit Gleichem“, nicht „Ähnliches mit Ähnlichen“ behandeln – ist zwar dem der Homöopathie sehr verwandt, ist aber eben nicht Homöopathie. Es wird zwar manchmal auch von Homöopathen angewandt. Dann gibt ein Arzt z.B. potenzierte Kuhmilch, wenn klar ist, dass Milch zu den Problemen führt und andere Arzneimittel nicht gut wirken. Aber klinisch gesehen ist diese isopathische Art der Anwendung, wie sie auch den Studien von Reilly zugrundeliegt, eher eine Randerscheinung. Praktisch-klinisch hat diese Studienreihe also wenig Bedeutung. Dafür ist es aber ein schönes, sauberes Forschungsmodell das beispielhaft zeigt, dass potenzierte Substanzen in einem klinischen Modell wirken können. Das ist überhaupt ein Forschungsdilemma, das auch in der konventionellen Forschung kaum wegzubekommen ist. Man kann es selten so haben, dass die Befunde wirklich für die angewandte, niedergelassene Praxis relevant sind und dass sie gleichzeitig wissenschaftlich sauber sind. Wir haben das vor Kurzem so ausgedrückt: Interne und externe Validität sind keine kompatiblen Konzepte, die in der gleichen Studie maximiert werden können. [3] Hier ist die interne Validität hoch, aber die externe Validität, also die Übertragbarkeit auf die Praxis eher niedrig. Dennoch, oder vielleicht deswegen, zeigt sie beispielhaft: Homöopathische Prinzipien sind offenbar weniger dumm, als manche meinen, und Homöopathie kann bei Allergien durchaus eine rationale Wahl sein, vor allem dann, wenn alles andere nicht gut funktioniert. Doch dann würde ich lieber klassische Homöopathie wählen, auch wenn diese hier nicht untersucht wurde. Das Prinzip hat sich nämlich bewährt.
Referenzen
[1] Reilly, D., Taylor, M. A., Beattie, N. G. M., Campbell, J. H., & McSharry, C. (1994). Is evidcence for homoeopathy reproducible? The Lancet, 344, 1601-1606.
[2] Taylor, M. A., Reilly, D., Llewellyn-Jones, R. H., McSharry, C., & Aitchison, T. C. (2000). Randomised controlled trial of homoeopathy versus placebo in perennial allergic rhinitis with overview of four trial series. British Medical Journal, 321, 471-476.
[3] Walach, H., & Loef, M. (2015). Using a matrix-analytical approach to synthesizing evidence solved incompatibility problem in the hierarchy of evidence. Journal of Clinical Epidemiology, 68, 1251-1260.
Bild
Trueffelpix stock.adobe.com

